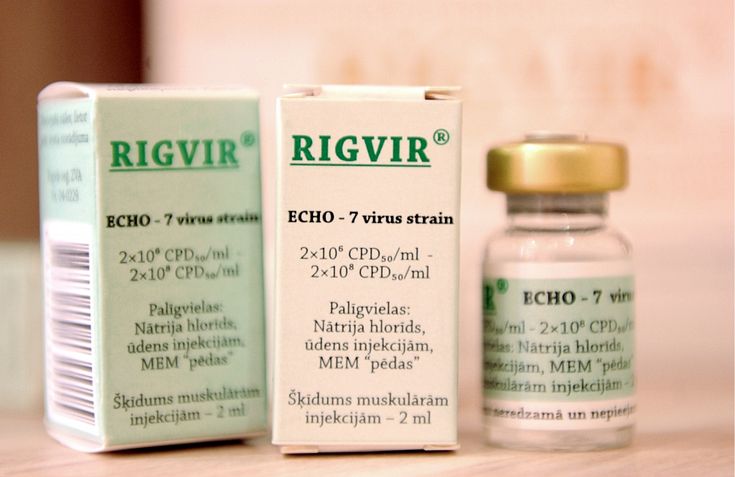
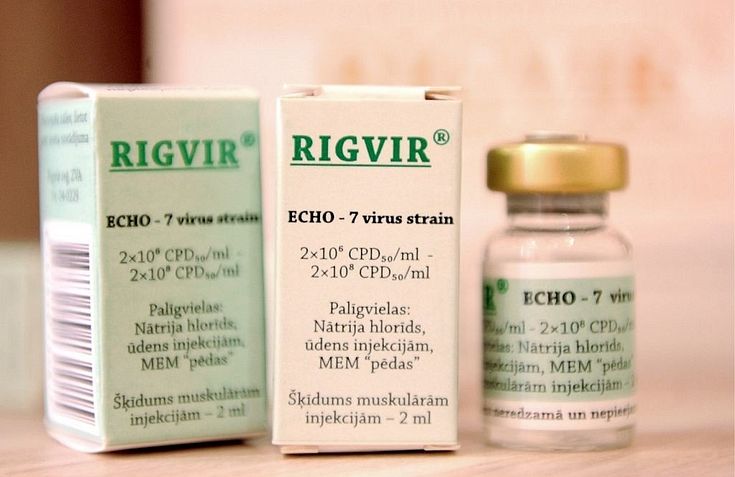
Biotehnoloģiju farmācijas uzņēmums «Rigvir grupa» patlaban konstatējis četru zāļu sēriju neatbilstību specifikācijai atbilstoši Latvijas Infektoloģijas centra (LIC) testu rezultātiem, informēja uzņēmumā.
Patlaban «Rigvir grupa» iesniegusi atbildīgajām valsts institūcijām izmeklēšanas starpziņojumu par pretvēža zāļu «Rigvir» pārbaudes rezultātiem. Konstatēto neatbilstību dēļ attiecīgo zāļu sēriju izplatīšana savlaicīgi apturēta.
Kā uzsvēra uzņēmumā, nav konstatēts apdraudējums pacientu veselībai un drošumam, bet «konstatēta nebūtiska un īstermiņa eventuāla ietekme uz terapeitisko efektivitāti nelielam zāļu daudzumam, kas ticis realizēts».
«Rigvir grupa» gan norāda uz neobjektivitāti, vērtējot Lielbritānijas NIBSC laboratorijā veiktos testus, jo tikušas izmantotas dažādas metodes un šūnu kultūras, līdz ar ko būtu jāveic salīdzinošie izmeklējumi, lai noskaidrotu rezultātu lielo atšķirību cēloņus. Uzņēmumam neesot arī pamata apšaubīt LIC testu rezultātus, jo LIC ir WHO akreditēta references laboratorija ar ilggadīgu pieredzi vīrusu titrēšanā un validētu metodi.
Uzņēmumā informēja - izmeklēšanā konstatēts, ka nav šaubu un risku attiecībā uz «Rigvir» ECHO-7 vīrusa identitāti un stabilitāti vai citiem apstākļiem, kas var izrietēt no vīrusa dabas un īpašībām, un arī NIBSC laboratorija sniegusi kvalitatīvu un profesionālu pozitīvu novērtējumu, ja neskaita lielās titru atšķirības.
Izmeklēšanā konstatēts, ka zāļu neatbilstība specifikācijai saistīta ar vairāku ārēju apstākļu kopumu, tostarp attiecībā uz uzglabāšanas nosacījumiem. Visas nepilnības un riski ir novēršami īstermiņā sadarbībā ar kontrolējošām institūcijām, uzskata «Rigvir grupa».
Kā iepriekš vēstīja Latvijas Televīzijas raidījums «de facto», «Rigvir» neatkarīgā pārbaudē secināts, ka vīruss, kam būtu jācīnās ar vēža šūnām, šķidrumā ir daudz mazākā apjomā, nekā apsolījis ražotājs. Latvijas Zāļu valsts aģentūras (ZVA) pasūtītā pārbaude veikta neatkarīgā laboratorijā Lielbritānijā.
ZVA zāļu ekspertīzes laboratorijas vadītāja vietnieks Guntars Kaspars pārbaudē atklāto salīdzinājis ar situāciju, kad, pērkot citronu sulu, tiek pārdots ūdens ar citrona grašu.
«Rigvir» partija, no kuras bija paraugs testēšanai, izņemta no apgrozījuma, taču pašu pārbaudi medikamenta ražotājs - biotehnoloģiju farmācijas uzņēmums «Rigvir grupa» - apšaubīja. Lai pārliecinātos, ka negatīvais rezultāts nebija nejaušs, ZVA nosūtījusi uz britu laboratoriju paraugus no vēl trīs dažādām «Rigvir» partijām.
Kaspars raidījumam teica, ka ir komersanti, kas uzreiz piekrīt pārbaužu rezultātiem un meklē neatbilstību cēloņus, bet ir arī komersanti, kas apstrīd pārbaužu rezultātus. «Tad mēs atkal ņemam papildu sērijas [jaunām pārbaudēm],» skaidroja Kaspars.
LTV ziņoja, ka atbilde par papildu paraugu testiem būs zināma marta beigās. Ja visiem trīs paraugiem rezultāti būs tikpat slikti kā pirmajā posmā, medikamentam draud aizliegums tos pārdot Latvijā un izslēgšana no kompensējamo medikamentu saraksta.
«Rigvir grupa» paziņoja, ka pati pēc savas iniciatīvas pieņēmusi «stratēģisku lēmumu uz nenoteiktu laiku apturēt nacionālajā reģistrācijas procedūrā reģistrēto zāļu «Rigvir» izplatīšanu Latvijas teritorijā nerentabilitātes dēļ».
«Rigvir grupa» uzņēmumu izpilddirektore Kristīne Jučkoviča raidījumam situāciju komentējusi, sakot, ka marta beigās kopā ar ZVA jautājums tiks risināts. Par sabiedrības veselību neesot jāuztraucas arī tad, ja pārbaudēs konstatētais būtu patiess. Uzņēmums gan tam nepiekrīt.
Medikamenta «Rigvir» iedarbība apšaubīta arī iepriekš, tostarp profesionālu ārstu, arī onkologu, organizācijas aicinājušas anulēt tā reģistrāciju valsts zāļu reģistrā.